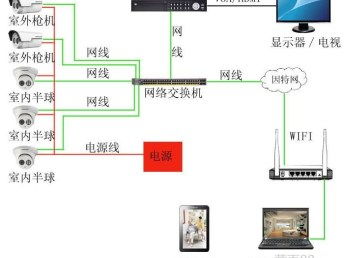
上海網絡工程培訓簽約就業班與虹口計算機二級培訓詳解

在當今數字化時代,網絡工程和計算機技能已成為職場競爭力的關鍵。上海搜課網絡推出的網絡工程培訓簽約就業班和虹口計算機二級培訓項目,為學員提供了全面、實用的學習平臺,助力個人職業發展。本文將詳細介紹這些培訓的介紹、產品、服務、圖片、價格及相關內容,涵蓋電腦培訓、網絡營銷、學歷教育等多個領域。
一、網絡工程培訓簽約就業班
網絡工程培訓簽約就業班專注于培養具備網絡設計、管理和維護能力的專業人才。課程內容涵蓋局域網與廣域網技術、網絡安全、服務器配置等核心模塊。學員通過理論學習和實戰操作,能夠掌握企業級網絡解決方案。該班級的特色在于簽約就業保障:學員完成培訓后,機構將協助推薦就業,確保學員順利進入IT行業。課程價格根據培訓時長和深度定制,通常從數千元至萬元不等,具體可咨詢上海搜課網絡獲取詳細信息。
二、虹口計算機二級培訓
虹口計算機二級培訓主要針對國家計算機等級考試(二級)進行輔導,內容包括計算機基礎知識、Office辦公軟件應用、程序設計基礎等。該培訓適合希望提升計算機操作能力或獲取證書的學生和職場人士。服務包括小班授課、模擬考試和個性化輔導,幫助學員高效備考。價格方面,標準課程一般在1000-3000元之間,具體視課程時長和附加服務而定。培訓機構通常會提供教材、在線資源和實操練習,確保學員通過考試。
三、產品與服務擴展
除了上述核心培訓,上海搜課網絡還提供多元化的教育產品,如網絡營銷課程,教授SEO、SEM等技能;學歷教育項目,協助學員提升學歷;藝術培訓、英語和小語種培訓,豐富個人素養;金融財會、建設工程培訓,針對專業領域深造;中小學輔導和出國留學服務,滿足各年齡段需求;以及高端研修班,為職場精英提供進階學習機會。這些課程均配有專業師資和實戰案例,圖片和資料可通過官網或咨詢獲取,讓學員直觀了解培訓環境。
四、計算機網絡工程的重要性
計算機網絡工程作為信息技術的基礎,廣泛應用于企業、政府和個人生活。學習網絡工程不僅能提升就業機會,還能推動數字化轉型。上海搜課網絡的培訓項目注重實踐與理論結合,通過項目驅動教學,幫助學員構建扎實的技能體系。無論是簽約就業班還是計算機二級培訓,都旨在培養適應市場需求的復合型人才。
上海網絡工程培訓簽約就業班和虹口計算機二級培訓為學員提供了可靠的學習路徑。選擇這些課程,不僅能獲得專業認證,還能通過簽約就業服務實現職業躍升。建議有意向者盡早咨詢,把握學習機會,開啟職業生涯新篇章。
如若轉載,請注明出處:http://m.leatherworld.cn/product/5.html
更新時間:2026-05-28 07:21:37